厦门泉州漳州莆田福州潮州汕头梅州龙岩三明宁德南平医疗器械管理体系ISO13485怎么办理?
(六)质量管理体系文件宣贯与试运行
体系文件制定批准后,需宣贯培训学习,试运行一段时间后才能生效正式使用。
(七)质量管理体系实施运行
1.实施程序:发布组织管理者的指令和质量管理体系文件,宣传和教育培训。
2.控制机制:协调各种质量活动,排除运行中的质量问题;可由自身、第二方或第三方监督质量体系的运行,及时获取质量信息并反馈问题;对质量体系的运行进行评价;上述组织协调、质量监控、质量信息管理、质量审核和评审、记录和考核等活动的过程和结果应及时准确记录,作为考核的依据。
(八)质量管理体系运行的不断改进
质量管理体系的建立不可能一蹴而就,一劳永逸,是一个不断完善,持续改进的过程。随着技术的发展、法律法规、企业实际情况等的变化都会存在不再适用的情况,因此要及时内审给予修订完善,不断改进。
四、医疗器械生产企业生产质量管理体系的构成。
根据医疗器械生产质量管理规范的要求,质量管理体系由以下方面构成。
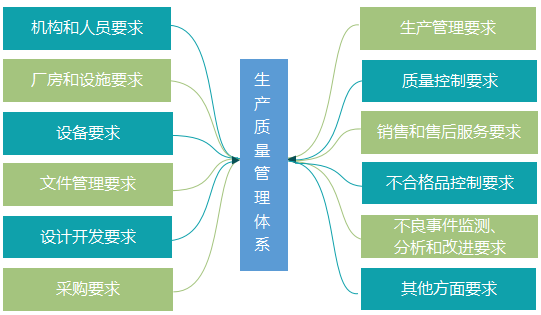
企业根据以上方面法规的具体要求(参见医疗器械生产质量管理规范现场检查指导原则),建立并实施质量管理体系,才能满足要求合规生产。
医疗器械生产质量管理体系是实现对医疗器械生产全过程控制,降低产品风险,保障医疗器械安全有效的重要手段,也是评价医疗器械质量的一项基本内容,医疗器械产品质量水平的高低大部分取决于企业质量体系水平的完善。因此,构建合理完善有效的医疗器械质量管理体系成为企业合规、健康、持续发展的重要手段。
